Виктоза, 6 мг/мл, раствор для подкожного введения, 3 мл, 2 шт.
| Действующее вещество | Лираглутид |
| Производитель | Novo Nordisk |
| Страна | Дания |
| Торговое название | Виктоза |
| Действующее вещество (МНН) | Лираглутид |
| Дозировка или размер | 6 мг/мл |
| Форма выпуска | раствор для подкожного введения |
| Первичная упаковка | картридж в шприц-ручке |
| Объём упаковки | 3 мл |
| Количество в упаковке | 2 |
| Производитель | Novo Nordisk |
| Страна | Дания |
| Срок годности | 30 мес |
| Условия хранения | При температуре 2–8 °C (в холодильнике) |
6 мг/мл, раствор для подкожного введения, 3 мл, 2 шт.
| Раствор для подкожного введения | 1 мл |
| активное вещество: | |
| лираглутид | 6 мг |
| (1 шприц-ручка (3 мл) содержит 18 мг лираглутида) | |
| вспомогательные вещества: натрия гидрофосфата дигидрат — 1,42 мг; пропиленгликоль — 14 мг; фенол — 5,5 мг; кислота хлористоводородная/натрия гидроксид — q.s.; вода для инъекций — до 1 мл |
Бесцветный или почти бесцветный прозрачный раствор.
Механизм действия
Лираглутид представляет собой аналог человеческого ГПП-1, произведенный методом биотехнологии рекомбинантной ДНК с использованием штамма Saccharomyces cerevisiae, имеющий 97% гомологичности с человеческим ГПП-1, который связывается и активирует рецепторы ГПП-1 у человека. Рецептор ГПП-1 служит мишенью для нативного ГПП-1 — эндогенного гормона инкретина, вызывающего стимуляцию глюкозозависимой секреции инсулина в бета-клетках поджелудочной железы. В отличие от нативного ГПП-1, фармакокинетический и фармакодинамический профили лираглутида позволяют вводить его пациентам 1 раз в сутки.
Профиль длительного действия лираглутида при п/к инъекции обеспечивается тремя механизмами: самоассоциацией, в результате которой происходит замедленное всасывание препарата; связыванием с альбумином и более высоким уровнем ферментативной стабильности по отношению к ДПП-4 и ферменту нейтральной эндопептидазы (НЭП), за счет чего обеспечивается длительный T1/2 препарата из плазмы. Действие лираглутида осуществляется за счет взаимодействия со специфическими рецепторами ГПП-1, в результате чего повышается уровень цАМФ. Под действием лираглутида происходит глюкозозависимая стимуляция секреции инсулина и улучшение функции бета-клеток поджелудочной железы. Одновременно лираглутид подавляет излишне высокую глюкозозависимую секрецию глюкагона. Таким образом, при повышении концентрации глюкозы крови происходит стимуляция секреции инсулина и подавление секреции глюкагона. С другой стороны, во время гипогликемии лираглутид снижает секрецию инсулина, но не подавляет секрецию глюкагона. Механизм снижения уровня гликемии включает также небольшую задержку опорожнения желудка. Лираглутид снижает массу тела и уменьшает жировую ткань при помощи механизмов, вызывающих уменьшение чувства голода и снижение расхода энергии.
ГПП-1 является физиологическим регулятором аппетита и потребления калорий, а рецепторы ГПП-1 расположены в нескольких областях головного мозга, участвующих в процессах регуляции аппетита.
В исследованиях на животных периферическое введение лираглутида приводило к захвату препарата в специфических областях головного мозга, включая гипоталамус, где лираглутид посредством специфической активации рецепторов ГПП-1 усиливал сигналы насыщения и ослаблял сигналы голода, тем самым приводя к уменьшению массы тела.
Исследования на экспериментальных животных моделях с предиабетом показали, что лираглутид замедляет развитие сахарного диабета. Диагностика in vitro показала, что лираглутид является мощным фактором специфической стимуляции пролиферации бета-клеток поджелудочной железы и предупреждает гибель бета-клеток (апоптоз), индуцируемую цитокинами и свободными жирными кислотами. In vivo лираглутид повышает биосинтез инсулина и увеличивает массу бета-клеток у экспериментальных животных моделей с сахарным диабетом. Когда концентрация глюкозы нормализуется, лираглутид перестает увеличивать массу бета-клеток поджелудочной железы.
Препарат Виктоза® обладает длительным 24-часовым действием и улучшает гликемический контроль путем снижения концентрации глюкозы крови натощак и после еды у пациентов с сахарным диабетом типа 2.
Глюкозозависимая секреция инсулина. При возрастании концентрации глюкозы в крови лираглутид увеличивает секрецию инсулина. При применении поэтапной инфузии глюкозы секреция инсулина после введения однократной дозы препарата Виктоза® пациентам с сахарным диабетом типа 2 возрастает до уровня, сопоставимого с таковым у здоровых субъектов (рис. 1).
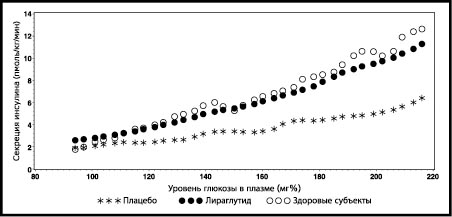
Рисунок 1. Средняя скорость секреции инсулина (ССИ) в сравнении с концентрацией глюкозы после введения однократной дозы 7,5 мкг/кг (»0,66 мг) или плацебо у пациентов с сахарным диабетом типа 2 (N=10) и у не получавших терапию здоровых субъектов (N=10) во время поэтапной инфузии глюкозы (исследование 2063)
Функция бета-клеток поджелудочной железы. Препарат Виктоза® улучшает функцию бета-клеток поджелудочной железы, что подтверждается первой и второй фазой инсулинового ответа и максимальной секреторной активностью бета-клеток. Фармакодинамические исследования пациентов с сахарным диабетом типа 2 показали восстановление первой фазы секреции инсулина (в/в введение инсулина), улучшение второй фазы секреции инсулина (гипергликемический клэмп-тест) и максимальную секреторную активность инсулина (тест стимуляции аргинином).
В ходе 52-недельной терапии препаратом Виктоза® произошло улучшение функции бета-клеток поджелудочной железы, что подтверждается оценкой гомеостатической модели функции бета-клеток поджелудочной железы (НОМА-индекс) и соотношением инсулина к проинсулину.
Секреция глюкагона. Препарат Виктоза®, стимулируя секрецию инсулина и подавляя секрецию глюкагона, уменьшает концентрацию глюкозы в крови. Препарат Виктоза® не подавляет глюкагоновый ответ на низкую концентрацию глюкозы. Кроме того, на фоне лираглутида наблюдается более низкая выработка эндогенной глюкозы.
Опорожнение желудка. Лираглутид вызывает небольшую задержку опорожнения желудка, что приводит к снижению интенсивности поступления постпрандиальной глюкозы в кровь.
Масса, состав тела и расход энергии. У субъектов с повышенной массой тела, включенных в долгосрочные клинические исследования препарата Виктоза®, последний вызывал значительное снижение массы тела. Сканирование при помощи методов КТ и двухэнергетической рентгеновской абсорбциометрии (ДЭРА) показало, что потеря массы тела произошла в первую очередь из-за потери жировой ткани пациентов. Эти результаты объясняются тем, что во время терапии препаратом Виктоза® у пациентов снижаются ощущение голода и расход энергии.
Электрофизиология сердца (ЭФс). Действие препарата Виктоза® на процесс реполяризации в сердце было протестировано в исследовании ЭФс. Применение препарата Виктоза® в равновесной концентрации в ежедневной дозе до 1,8 мг не продуцирует удлинение скорректированного интервала QT.
Клиническая эффективность. 3992 пациента с диабетом типа 2 были рандомизированы в 5 двойных слепых клинических исследований по безопасности и эффективности, осуществленных в целях оценки влияния препарата Виктоза® на гликемический контроль. Терапия препаратом Виктоза® вызывает клинически и статистически значимое улучшение показателя HbA1с, концентрации глюкозы натощак и постпрандиальной глюкозы по сравнению с плацебо.
Эти исследования включали 3978 получивших терапию пациентов (2501 пациент получал терапию препаратом Виктоза®), 53,7% мужчин и 46,3% женщин, у 797 пациентов (508 получили терапию препаратом Виктоза®) возраст составил ≥65 лет, у 113 пациентов (66 получили терапию препаратом Виктоза®) возраст составил ≥75 лет.
Гликемический контроль. Препарат Виктоза® в виде монотерапии в течение 52 нед вызывает статистически значимое (p<0,0014) и продолжительное снижение показателя HbA1с по сравнению с этим же показателем у пациентов, получающих терапию глимепиридом. При этом отмеченное снижение HbA1с ниже уровня 7% сохраняется на протяжении 12 мес (рис. 2).
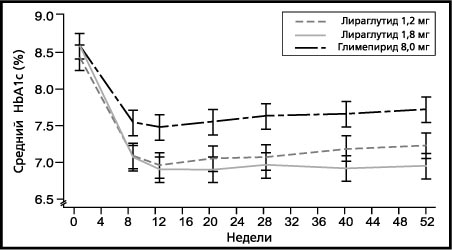
Рисунок 2. Уровень HbA1с составил менее 7% и сохранялся на протяжении 12 мес при назначении препарата Виктоза® пациентам, ранее получавшим терапию в виде диеты и физических нагрузок (исследование 1573)
У пациентов с HbA1с выше уровня 9,5% в исходной точке исследования данный показатель снизился на 2,1% на фоне монотерапии препаратом Виктоза®, в то время как у пациентов, участвующих в комбинированных клинических исследованиях препарата Виктоза®, средний уровень HbA1с снизился на 1,1–2,5%.
Препарат Виктоза® в течение 26-недельной комбинированной терапии с метформином, препаратами сульфонилмочевины или метформином и тиазолидиндионом вызывает статистически значимое (р<0,0001) и продолжительное снижение уровня НbА1с по сравнению с таковым у пациентов, получающих плацебо.
У пациентов, не достигших адекватного гликемического контроля на терапии препаратом Виктоза® и метформином, добавление инсулина детемир обеспечило бóльшую эффективность по сравнению с терапией препаратом Виктоза® и метформином после 26 нед лечения (снижение уровня HbA1с на 0,52%).
Было доказано, что эффективность препарата Виктоза® в дозе 0,6 мг в комбинации с препаратами сульфонилмочевины или метформином превосходит плацебо, но в то же время является более низкой по сравнению с дозировками 1,2 и 1,8 мг.
Соотношение пациентов, достигших снижения уровня HbA1с. На фоне монотерапии препаратом Виктоза® в течение 52-недельного исследования число пациентов, достигших уровня НbА1с <7%, статистически значимо выросло (р≤0,0007) по сравнению с числом пациентов, получающих глимепирид. На 26-й нед применения препарата Виктоза® в сочетании с метформином, препаратами производных сульфонилмочевины или комбинацией метформина с тиазолидиндионами число пациентов, достигших уровня НbА1с ≤6,5%, статистически значимо выросло (р≤0,0001) по отношению к числу пациентов, которые получали терапию гипогликемическими препаратами без добавления препарата Виктоза®.
В группах пациентов, не достигших адекватного гликемического контроля на терапии препаратом Виктоза® и метформином, процентное соотношение пациентов, достигших целевого уровня HbA1с (<7 и ≤6,5%) было значительно выше при терапии инсулин детемир + лираглутид 1,8 мг + метформин по сравнению с терапией лираглутид 1,8 мг + метформин (р≤0,0001/р=0,0016).
В ходе 26-недельного исследования комбинированного применения препарата Виктоза® удалось достичь показателя НbА1с <7% у большего числа пациентов, получавших препарат в виде комбинированной терапии, по сравнению с числом пациентов, получавших его в виде монотерапии.
Пациенты с нарушением функции почек. В двойном слепом исследовании эффективности и безопасности препарата Виктоза® 1,8 мг по сравнению с плацебо в качестве дополнения к инсулину и/или пероральным сахароснижающим препаратам у пациентов с сахарным диабетом типа 2 и нарушением функции почек умеренной степени препарат Виктоза® был более эффективен в снижении уровня HbA1с через 26 нед (-1,05% в сравнении с -0,38%, р<0,0001). У значимо большего количества пациентов было достигнуто значение HbA1с меньше 7% при применении препарата Виктоза® по сравнению с применением плацебо (52,8% в сравнении с 19,5%; р<0,0001). У пациентов, получавших препарат Виктоза®, было отмечено статистически значимое снижение массы тела по сравнению с пациентами, получавшими плацебо (-2,41 кг в сравнении с -1,09 кг, р=0,0052). Риск развития эпизодов гипогликемии между двумя группами терапии был сопоставим. Профиль безопасности препарата Виктоза® был, в целом, аналогичен отмеченному в других исследованиях препарата Виктоза®.
Уровень гликемии натощак. Концентрация глюкозы натощак снизилась на 13–43,5 мг% (0,72–2,42 ммоль/л) на фоне приема препарата Виктоза® как в виде монотерапии, так и в комбинации с одним или двумя пероральными гипогликемическими средствами. Это снижение наблюдалось уже в течение первых двух недель лечения.
Постпрандиальный уровень гликемии. При применении препарата Виктоза® наблюдалось снижение концентрации постпрандиальной глюкозы после каждого из трех ежедневных приемов пищи на 31–49 мг% (1,68–2,71 ммоль/л).
Масса тела. 52-недельная монотерапия препаратом Виктоза® ассоциировалась с устойчивым снижением массы тела.
На протяжении всего периода клинического исследования устойчивое снижение массы тела также ассоциировалось с применением препарата Виктоза® в комбинации с метформином и в сочетании с комбинациями метформина с производными сульфонилмочевины или метформина с тиазолидиндионом.
Снижение массы тела у пациентов, получающих препарат Виктоза® в комбинации с метформином, также наблюдалось после добавления инсулина детемир.
Наибольшее снижение массы тела наблюдалось у пациентов, имевших в исходной точке исследования повышенный ИМТ.
Монотерапия препаратом Виктоза® в течение 52 нед вызвала уменьшение среднего объема талии на 3–3,6 см.
Снижение массы тела наблюдалось у всех пациентов, получавших терапию препаратом Виктоза®, независимо от того, испытывали они или нет побочную реакцию в виде тошноты.
Препарат Виктоза® в составе комбинированной терапии с метформином снизил объем подкожно-жировой клетчатки на 13–17%.
Неалкогольный стеатогепатоз. Лираглутид уменьшает выраженность стеатогепатоза у пациентов с сахарным диабетом типа 2.
Иммуногенность. Учитывая возможность иммуногенного влияния белковых и пептидных лекарственных препаратов, применение препарата Виктоза® у пациентов может привести к образованию антител к лираглутиду. Образование антител отмечается в среднем у 8,6% пациентов. Образование антител не приводит к снижению эффективности препарата Виктоза®.
Оценка влияния на ССС. Долгосрочные клинические исследования показали, что препарат Виктоза® снижает показатели сАД в среднем на 2,3–6,7 мм рт. ст. в первые 2 нед лечения. Препарат Виктоза® понижал частоту развития метаболического синдрома в соответствии с определением III доклада группы экспертов по лечению взрослых (АТРIII). Снижение сАД происходило до снижения массы тела.
В ретроспективном анализе серьезных нежелательных явлений со стороны ССС (смерть по причине сердечно-сосудистой патологии, инфаркт миокарда, инсульт) по данным всех долгосрочных исследований и исследований средней продолжительности II и III фазы (продолжительностью от 26 до 100 нед), включавших 5607 пациентов (3651 пациент получал препарат Виктоза®), было продемонстрировано отсутствие увеличения сердечно-сосудистого риска (отношение коэффициентов заболеваемости 0,75 (95% ДИ 0,35; 1,63) в отношении комбинированной конечной точки при применении препарата Виктоза® в отличии от всех препаратов сравнения (метформин, глимепирид, росиглитазон, инсулин гларгин, плацебо). Пациенты с высоким сердечно-сосудистым риском были исключены из исследований, и частота серьезных сердечно-сосудистых явлений в исследованиях была низкой (6,02 на 1000 пациенто-лет у получавших препарат Виктоза® пациентов и 10,45 — у пациентов, получавших все препараты сравнения), что препятствует получению однозначных выводов.
Другие клинические данные. В открытом исследовании, в котором проводили сравнение эффективности и безопасности препарата Виктоза® в дозе 1,8 мг и ликсисенатида в дозе 20 мкг у 404 пациентов с неудовлетворительным контролем гликемии на фоне терапии метформином (среднее значение HbA1с 8,4%), препарат Виктоза® более эффективно снижал уровень HbA1с по сравнению с ликсисенатидом через 26 нед терапии (-1,83% в сравнении с -1,21%, р<0,0001). У значительно большего количества пациентов было достигнуто значение HbA1с <7% при применении препарата Виктоза® по сравнению с ликсисенатидом (74,2% в сравнении с 45,5%, р<0,0001), а также целевое значение HbA1с 6,5% или меньше (54,6% в сравнении с 26,2%, р<0,0001). Значительно более выраженное снижение концентрации глюкозы плазмы натощак было достигнуто при применении препарата Виктоза®по сравнению с ликсисенатидом (-2,85 в сравнении с -1,70 ммоль/л, р<0,0001). Снижение массы тела было отмечено в обеих группах терапии (-4,3 кг при применении препарата Виктоза® и -3,7 кг при применении ликсисенатида). Профиль безопасности препарата Виктоза® и ликсисенатида был, в целом, сопоставим. Не было выявлено новой информации по безопасности при применении препарата Виктоза®.
В сравнительном исследовании эффективности и безопасности препарата Виктоза® (в дозах 1,2 и 1,8 мг) и ингибитора ДПП-4 ситаглиптина в дозе 100 мг у пациентов, не достигших адекватного контроля на терапии метформином, после 26 нед лечения доказано лучшее снижение показателя HbA1с при применении препарата Виктоза® в обеих дозах по сравнению с ситаглиптином (-1,24, -1,5% по сравнению с -0,9%, р<0,0001). Значительно большее количество пациентов достигли показателя HbA1с ниже 7% при применении препарата Виктоза® по сравнению с ситаглиптином (43,7 и 56% по сравнению с 22%, р<0,0001). Снижение массы тела у пациентов, получавших препарат Виктоза®, было значительно больше по сравнению с пациентами, получавшими ситаглиптин (-2,9 и -3,4 кг в сравнении с -1 кг, р<0,0001). По сравнению с пациентами, получавшими ситаглиптин, у пациентов, получавших препарат Виктоза®, чаще отмечалась тошнота. Однако тошнота была преходящей.
Частота случаев легкой гипогликемии незначительно отличалась при лечении препаратом Виктоза® и ситаглиптином (0,178 и 0,161 в сравнении с 0,106 случая/пациента в год). Снижение показателя HbA1с и преимущество препарата Виктоза® по сравнению с ситаглиптином, наблюдавшееся после 26 нед лечения препаратом Виктоза® (1,2 и 1,8 мг), сохранялось после 52 нед лечения (-1,29 и -1,51% в сравнении с -0,88%, р<0,0001). После 52 нед применения ситаглиптина пациенты были переведены на препарат Виктоза®, что привело к дополнительному и статистически значимому снижению показателя HbA1с на 78-й нед лечения (0,24 и 0,45%, 95 ДИ: от 0,41 до 0,07 и от -0,67 до 0,23), но контрольная группа пациентов не была доступна.
В сравнительном исследовании эффективности и безопасности препарата Виктоза® (в дозе 1,8 мг) и эксенатида (в дозе 10 мкг 2 раза в день) у пациентов, не достигших адекватного контроля на терапии метформином и/или производными сульфонилмочевины, после 26 нед применения препарата Виктоза® отмечено большее снижение показателя HbA1с по сравнению с эксенатидом (-1,12% в сравнении с -0,79%, р<0,0001). Значительно большее количество пациентов достигли показателя HbA1с ниже 7% на терапии препаратом Виктоза® по сравнению с эксенатидом (54,2% по сравнению с 43,4%, р=0,0015). Обе терапии показали среднюю потерю массы тела — приблизительно 3 кг.
Количество пациентов, сообщавших о тошноте, было ниже в группе пациентов, получавших препарат Виктоза®, по сравнению с эксенатидом. Частота случаев легкой гипогликемии была значительно ниже в группе пациентов, получавших препарат Виктоза®, по сравнению с эксенатидом (1,932 в сравнении с 2,6 случая/пациента в год, р=0,01). Через 26 нед применения эксенатида пациенты были переведены на препарат Виктоза®, что привело к дополнительному снижению показателя HbA1с на 40-й нед лечения (-0,32%, р<0,0001), при этом 13% пациентов удалось достичь показателя HbA1с ниже 7%.
Терапия препаратом Виктоза® в течение 52 нед улучшила инсулиночувствительность по сравнению с таковой у препаратов сульфонилмочевины, что было выявлено при помощи гомеостатической модели оценки инсулинорезистентности HOMA-IR.
Абсорбция. Всасывание лираглутида после п/к введения происходит медленно, Tmax в плазме — 8–12 ч после введения дозы препарата. Cmax лираглутида в плазме после п/к инъекции в однократной дозе 0,6 мг составляет 9,4 нмоль/л. При введении лираглутида в дозе 1,8 мг средний показатель его Css в плазме (AUCτ/24) достигает приблизительно 34 нмоль/л. Экспозиция лираглутида (процесс воздействия препарата) усиливается пропорционально введенной дозе. После введения лираглутида в однократной дозе внутрииндивидуальный коэффициент вариации для AUC составляет 11%. Абсолютная биодоступность лираглутида после п/к введения составляет приблизительно 55%.
Распределение. Кажущийся Vd лираглутида в тканях после п/к введения — 11–17 л. Средний Vd лираглутида после в/в введения — 0,07 л/кг. Лираглутид в значительной степени связывается с белками плазмы крови (>98%).
Метаболизм. На протяжении 24 ч после введения здоровым добровольцам однократной дозы меченного радиоактивным изотопом (3H)-лираглутида главным компонентом плазмы оставался неизмененный лираглутид. Были обнаружены два метаболита в плазме (≤9 и ≤5% от уровня общей радиоактивности в плазме крови). Лираглутид метаболизируется подобно крупным белкам, без участия какого-либо специфического органа в качестве пути выведения.
Выведение. После введения дозы (3H)-лираглутида неизмененный лираглутид не определялся в моче или кале. Лишь незначительная часть введенной радиоактивности в виде связанных с лираглутидом метаболитов (6 и 5% соответственно) выводилась почками или через кишечник. Радиоактивные вещества почками или через кишечник выводятся в основном в течение первых 6–8 дней после введения дозы препарата и представляют собой три метаболита. Средний клиренс из организма после п/к введения лираглутида в однократной дозе составляет приблизительно 1,2 л/ч с элиминационным T1/2 примерно 13 ч.
Особые группы пациентов
Пожилой возраст: данные фармакокинетических исследований в группе здоровых добровольцев и анализ фармакокинетических данных, полученных в популяции пациентов от 18 до 80 лет, свидетельствуют о том, что возраст не оказывает клинически значимого эффекта на фармакокинетические свойства лираглутида.
Пол: популяционный фармакокинетический анализ данных, полученных при исследовании действия лираглутида у пациентов женского и мужского пола, и данные фармакокинетических исследований в группе здоровых добровольцев свидетельствуют о том, что пол не оказывает клинически значимый эффект на фармакокинетические свойства лираглутида.
Этническая принадлежность: популяционный фармакокинетический анализ данных, полученных при исследовании действия лираглутида у субъектов белой, черной, азиатской и латиноамериканской расовых групп, свидетельствует о том, что этническая принадлежность не оказывает клинически значимый эффект на фармакокинетические свойства лираглутида.
Ожирение: популяционный фармакокинетический анализ данных свидетельствует о том, что ИМТ не оказывает клинически значимый эффект на фармакокинетические свойства лираглутида.
Печеночная недостаточность: фармакокинетические свойства лираглутида исследовались в ходе клинического исследования однократной дозы препарата у субъектов с различной степенью печеночной недостаточности. В исследование были включены пациенты с печеночной недостаточностью легкой степени (по классификации Child Pugh тяжесть заболевания 5–6 баллов) и тяжелой печеночной недостаточностью (по классификации Child Pugh тяжесть заболевания >9 баллов). Экспозиция лираглутида в группе пациентов с нарушениями функции печени была не выше, чем таковая в группе здоровых субъектов, что указывает на то, что печеночная недостаточность не оказывает клинически значимый эффект на фармакокинетику лираглутида.
Почечная недостаточность: фармакокинетика лираглутида изучалась у пациентов с различной степенью почечной недостаточности в исследовании однократной дозы. В данное исследование были включены субъекты с различной степенью почечной недостаточности: от легкой (оценка Cl креатинина 50–80 мл/мин) до тяжелой (оценка Cl креатинина <30 мл/мин) и субъекты с терминальной стадией почечной недостаточности, нуждающиеся в гемодиализе. Почечная недостаточность не оказала клинически значимый эффект на фармакокинетику лираглутида.
Дети: исследование препарата Виктоза® у детей не проводилось.
Данные доклинического исследования безопасности
Доклинические данные, основанные на исследованиях фармакологической безопасности, токсичности повторных доз и генотоксичности, не выявили какой-либо опасности для человека.
В двухлетних исследованиях канцерогенности были выявлены опухоли С-клеток щитовидной железы крыс и мышей, не приводившие к летальному исходу. Нетоксическая доза (NOAEL) у крыс не установлена. Появление подобных опухолей у обезьян, получавших терапию лираглутидом в течение 20 мес, не отмечалось.
Результаты, полученные в ходе испытаний на грызунах, связаны с тем, что грызуны проявляют особую чувствительность в отношении опосредуемого рецептором ГПП-1 негенотоксичного специфического механизма. Значимость полученных данных для человека является низкой, однако не может быть полностью исключена. Появления каких-либо других новообразований, связанных с проводимой терапией, не отмечалось.
В исследованиях на животных не выявлен прямой неблагоприятныый эффект препарата на фертильность, но отмечено незначительное увеличение частоты ранней эмбриональной смерти при лечении самой высокой дозой препарата. Введение препарата Виктоза® крысам в середине периода беременности вызвало у них сокращение массы тела самки и роста эмбриона с не изученным до конца эффектом на ребра, а в группе кроликов — отклонения в скелетной структуре. Рост новорожденных особей в группе крыс во время терапии препаратом Виктоза® снизился, и это снижение устойчиво сохранялось в период после окончания грудного вскармливания в группе моделей, получавших высокие дозы лираглутида. Неизвестно, обусловлен ли этот эффект снижением потребления калорий вследствие прямого влияния ГПП-1.
Препарат Виктоза® показан у взрослых пациентов с сахарным диабетом типа 2 на фоне диеты и физических упражнений для достижения гликемического контроля в качестве:
— монотерапии;
— комбинированной терапии с одним или несколькими пероральными гипогликемическими препаратами (с метформином, производными сульфонилмочевины или тиазолидиндионами), у пациентов, не достигших адекватного гликемического контроля на предшествующей терапии;
— комбинированной терапии с базальным инсулином у пациентов, не достигших адекватного гликемического контроля на терапии препаратом Виктоза® и метформином.
Перед началом использования шприц-ручки Виктоза® следует тщательно изучить указанную инструкцию.
Шприц-ручка Виктоза® содержит 18 мг лираглутида. Пациент может выбрать любую из трех возможных дозировок: 0,6, 1,2 и 1,8 мг. Шприц-ручка Виктоза® предназначена для использования в комбинации с одноразовыми иглами НовоФайн® или НовоТвист® длиной до 8 мм и толщиной до 32G (0,25/0,23 мм).
Шприц-ручка Виктоза®
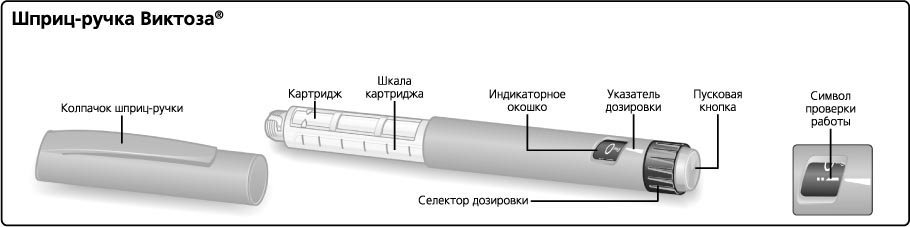
Игла (пример)
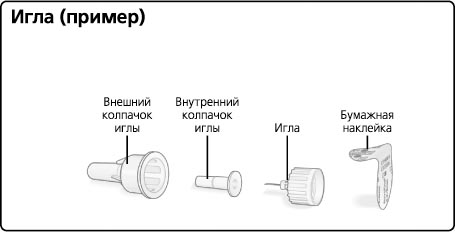
Подготовка шприц-ручки к инъекции
Проверьте название и цветовой код на этикетке шприц-ручки, чтобы убедиться, что в ней содержится лираглутид. Применение неправильного препарата может быть вредным для здоровья пациента.
А. Снять колпачок со шприц-ручки.
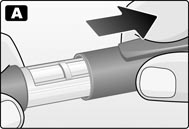
B. Снять с одноразовой иглы бумажную наклейку. Аккуратно и плотно накрутить иглу на шприц-ручку.
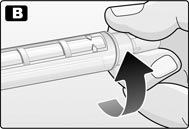
C. Снять внешний колпачок иглы и отложить его в сторону, не выбрасывая.
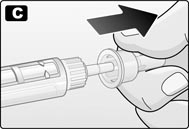
D. Снять внутренний колпачок иглы и выбросить его.
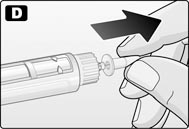
Важная информация. При каждой инъекции всегда использовать новую иглу. Такая мера позволит предотвратить загрязнение, инфицирование, утечку препарата из шприц-ручки, закупорку игл и гарантирует точность дозирования.
Важная информация. Соблюдать меры предосторожности в обращении с иглой, чтобы не допутить изгиба или повреждения иглы перед ее использованием.
Важная информация. Никогда не надевать внутренний колпачок обратно на иглу. Это предотвратит риск случайного укола иглой.
Уход за шприц-ручкой
— не пытаться самостоятельно починить шприц-ручку или разобрать ее на части;
— предохранять шприц-ручку от попадания пыли, загрязнений и всех видов жидкостей;
— шприц-ручку можно очищать тканью, смоченной мягким моющим средством. Не погружать шприц-ручку в воду, не мыть и не смазывать ее, т.к. это может повредить механизм.
Важная информация
Шприц-ручка предназначена для индивидуального использования — не следует передавать ее другим лицам. Хранить шприц-ручку в недоступном для всех, а в особенности для детей, месте.
Проверка работы шприц-ручки
Важная информация.
Всегда производить проверку работы шприц-ручки, как показано ниже, прежде, чем использовать новую шприц-ручку для инъекций.
Если пациент уже использует шприц-ручку, ему следует перейти к этапу Н «Установка дозы».
Важная информация.
E. Поворачивать селектор дозировки до тех пор, пока в индикаторном окошке символ проверки работы не поравняется с указателем дозировки.
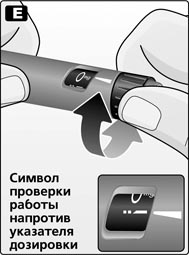
F. Держа шприц-ручку иглой вверх, несколько раз постучать по картриджу пальцем, чтобы пузырьки воздуха переместились в верхнюю часть картриджа.
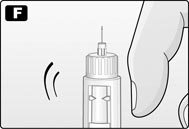
G. Удерживая шприц-ручку иглой вверх, нажимать пусковую кнопку до тех пор, пока в индикаторном окошке напротив указателя дозировки не появится 0 мг. На конце иглы должна появиться капля раствора лираглутида. Если капля не появилась, повторять операции Е–G до тех пор, пока на конце иглы не появится капля лираглутида. Если после 4 повторов указанных операций капля препарата на конце иглы так и не появилась, поменять иглу на новую и повторить операции Е–G еще раз. Если капля препарата на конце иглы так и не появилась, это означает, что шприц-ручка неисправна и пациенту следует использовать новую шприц-ручку.
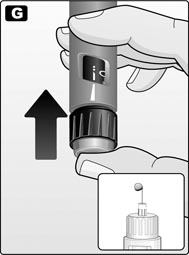
Важная информация. Если пациент уронил шприц-ручку на твердую поверхность или у него появились сомнения в ее полной исправности, прежде чем начать введение препарата, необходимо прикрепить новую одноразовую иглу и осуществить проверку работы шприц-ручки.
Установка дозы
Прежде всего необходимо удостовериться, что в индикаторном окошке «0 мг» находится напротив указателя дозировки.
H. Поворачивать селектор дозировки до тех пор, пока нужная пациенту доза (0,6; 1,2 или 1,8 мг) в индикаторном окошке не поравняется с указателем дозировки (mg означает мг). Исправить ошибочно установленную дозу можно путем вращения селектора дозировки вперед или назад до тех пор, пока цифры нужной дозы в индикаторном окошке не поравняются с указателем дозировки. При вращении селектора дозировки назад соблюдать осторожность, чтобы случайно не нажать на пусковую кнопку, во избежание выброса дозы лираглутида. Если селектор дозировки остановился до того, как в индикаторном окошке напротив указателя дозировки появилась нужная пациенту доза, это означает, что оставшегося в шприц-ручке лираглутида не хватает для введения полной дозы. В таком случае вам следует выполнить одно из двух описанных ниже действий.
Ввести нужную дозу в два приема
Вращать селектор дозировки в любом направлении до тех пор, пока доза 0,6 или 1,2 мг не окажется напротив указателя дозировки. Сделать инъекцию. Подготовить новую шприц-ручку для второй инъекции и ввести остаток дозы препарата (в миллиграммах) для того, чтобы завершить введение полной дозы. Можно разделить дозу препарата между используемой и новой шприц-ручкой только, если пациента этому обучили или если это рекомендовал врач. Необходимо использовать калькулятор для планирования доз. Если пациент неправильно разделит дозу, он может ввести недостаточное или слишком большое количество лираглутида.
Сделать инъекцию полной дозы препарата с помощью новой шприц-ручки
Если селектор дозировки остановился до того, как в индикаторном окошке напротив указателя дозировки появились цифры 0,6 мг, подготовить для инъекции новую шприц-ручку и ввести полную дозу препарата с помощью новой шприц-ручки.
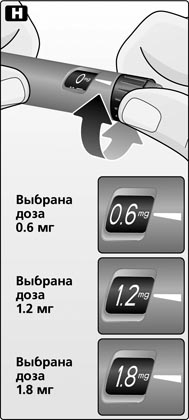
Важная информация. Не пытаться выбрать другие дозы, кроме доз 0,6; 1,2 или 1,8 мг. Цифры в индикаторном окошке должны находиться точно напротив указателя дозировки — такое положение гарантирует, что пациент получит правильную дозу препарата.
Селектор дозировки при вращении издает щелчки. Не использовать эти щелчки для отмеривания дозы лираглутида, необходимой пациенту для инъекции.
Не использовать шкалу картриджа для отмеривания дозы лираглутида для инъекции — она показывает недостаточно точные значения.
Введение препарата
Ввести иглу под кожу, используя технику инъекций, рекомендованную врачом или медсестрой. Затем следовать инструкциям, данным ниже:
I. Нажать пусковую кнопку до упора, пока в индикаторном окошке напротив указателя дозировки не появится «0 мг». Необходимо соблюдать осторожность: не дотрагиваться пальцами до индикаторного окошка и не нажимать на селектор дозировки — это может вызвать блокировку механизма шприц-ручки. Держать пусковую кнопку в нажатом до упора состоянии, а иглу под кожей в течение минимум 6 с. Это обеспечит введение полной дозы препарата.
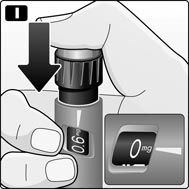
J. Извлечь иглу из-под кожи. Пациент может увидеть каплю лираглутида на конце иглы. Это нормальное явление, которое никак не влияет на дозу препарата, которая была только что введена.
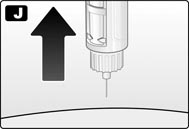
K. Ввести конец иглы внутрь внешнего колпачка иглы, не дотрагиваясь до него.
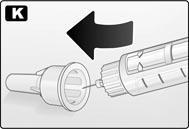
L. Когда игла находится в колпачке, осторожно подтолкнуть внешний колпачок иглы вперед, чтобы игла полностью вошла в него. Затем отвинтить иглу. Выбросить иглу, соблюдая меры предосторожности, и закрыть шприц-ручку колпачком. Если же шприц-ручка пуста, отвинтить иглу и выбросить пустую шприц-ручку без иглы. Соблюдать местные требования к утилизации использованных медицинских материалов.
Важная информация. Удалять использованную иглу после каждой инъекции и не хранить шприц-ручку с присоединенной иглой.
Важная информация. Это поможет предотвратить загрязнение, инфицирование и утечку лираглутида из шприц-ручки из шприц-ручки и закупорку игл. Кроме того, это обеспечит точность дозировки.
Важная информация.Лица, осуществляющие уход за больным, должны обращаться с использованными иглами с особой осторожностью, чтобы избежать случайных уколов и перекрестного инфицирования.
П/к в область живота, бедра или плеча, 1 раз в сутки в любое время, независимо от приема пищи. Место и время инъекции могут изменяться без коррекции дозы. Однако предпочтительнее вводить препарат приблизительно в одно и то же время суток, в наиболее удобное для пациента время. Дальнейшая информация по способу применения препарата Виктоза® содержится в разделе Руководство по использованию. Препарат Виктоза® нельзя вводить в/в и в/м.
Дозы
Начальная доза препарата — 0,6 мг лираглутида в день. После применения препарата в течение минимум 1 нед дозу следует увеличить до 1,2 мг. Есть данные о том, что у некоторых пациентов эффективность лечения возрастает при увеличении дозы препарата с 1,2 до 1,8 мг. Для достижения наилучшего гликемического контроля у больного с учетом клинической эффективности дозу препарата Виктоза® можно увеличить до 1,8 мг после применения его в дозе 1,2 мг в течение минимум 1 нед. Применение препарата в ежедневной дозе выше 1,8 мг не рекомендуется.
Препарат Виктоза® можно применять дополнительно к существующей терапии метформином или комбинированной терапии метформином с тиазолидиндионом. Терапию метформином и тиазолидиндионом можно продолжить в прежних дозах.
Препарат Виктоза® можно добавлять к проводимой терапии производными сульфонилмочевины или к комбинированной терапии метформином с производными сульфонилмочевины.
При добавлении препарата Виктоза® к терапии производными сульфонилмочевины следует учитывать снижение дозы производных сульфонилмочевины с целью минимизации риска возникновения нежелательных гипогликемий (см. «Особые указания»).
При добавлении препарата Виктоза® к терапии базальным инсулином следует учитывать снижение дозы инсулина с целью минимизации риска возникновения гипогликемии (см. «Особые указания»).
Для коррекции дозы препарата Виктоза® не требуется проведение самоконтроля глюкозы крови. Однако в начале терапии препаратом Виктоза® в комбинации с производными сульфонилмочевины или базальным инсулином такой самоконтроль глюкозы крови может потребоваться для коррекции дозы производных сульфонилмочевины или базального инсулина.
Пропущенная доза. В случае пропуска дозы препарат Виктоза® следует ввести как можно быстрее в пределах 12 ч с момента запланированного введения дозы.
Если продолжительность пропуска составляет более 12 ч, препарат Виктоза® следует ввести на следующий день в запланированное время.
Не следует вводить на следующий день дополнительную или увеличенную дозу препарата Виктоза® для компенсации пропущенной дозы.
Особые группы пациентов
Пожилой возраст (>65 лет): не требуется коррекция дозы в зависимости от возраста. Имеется ограниченный опыт применения препарата у пациентов в возрасте 75 лет и старше (см. «Фармакокинетика»).
Почечная недостаточность: не требуется коррекция дозы для пациентов, страдающих почечной недостаточностью легкой или средней степени тяжести (Cl креатинина 60–90 и 30–59 мл/мин, соответственно). Опыт применения препарата у пациентов с тяжелой почечной недостаточностью (Cl креатинина ниже 30 мл/мин) отсутствует. В настоящее время применение препарата Виктоза® у пациентов с тяжелыми нарушениями функции почек, в т.ч. с терминальной стадией почечной недостаточности, противопоказано (см. «Фармакокинетика»).
Печеночная недостаточность. В настоящее время имеется ограниченный опыт применения препарата Виктоза® у пациентов с печеночной недостаточностью, поэтому противопоказано применять его у пациентов с печеночной недостаточностью легкой, умеренной или тяжелой степени (см. «Фармакокинетика»).
Дети и подростки: Применение препарата Виктоза® у детей и подростков в возрасте до 18 лет противопоказано в связи с отсутствием данных по безопасности и эффективности.
Адекватные данные по применению препарата Виктоза® у беременных женщин отсутствуют. Исследования на животных продемонстрировали репродуктивную токсичность препарата (см. «Фармакокинетика», Данные доклинического исследования безопасности). Потенциальный риск для людей неизвестен.
Противопоказано применять препарат Виктоза® во время беременности, вместо него рекомендуется проводить лечение инсулином. Если пациентка готовится к беременности либо беременность уже наступила, терапию препаратом Виктоза® необходимо немедленно прекратить.
Неизвестно, проникает ли лираглутид в грудное молоко женщин. Исследования на животных показали, что проникновение лираглутида и метаболитов близкой структурной связи в грудное молоко является низким. Опыт применения препарата Виктоза® у кормящих женщин отсутствует. Применение препарата в период грудного вскармливания противопоказано.
повышенная чувствительность к активному веществу или другим компонентам, входящим в состав препарата;
медуллярный рак щитовидной железы в анамнезе, в т.ч. семейном;
множественная эндокринная неоплазия типа 2.
Противопоказано применение препарата Виктоза® у следующих групп пациентов и при следующих состояниях/заболеваниях в связи с отсутствием данных по эффективности и безопасности:
сахарный диабет типа 1;
диабетический кетоацидоз (см. «Особые указания»);
беременность и период грудного вскармливания (см. «Применение при беременности и кормлении грудью»);
тяжелые нарушения функции почек;
нарушения функции печени;
хроническая сердечная недостаточность III–IV функционального класса (в соответствии с классификацией NYHA (Нью-Йоркская кардиологическая ассоциация);
воспалительные заболевания кишечника (см.«Особые указания»);
диабетический гастропарез (см. «Особые указания»);
детский возраст до 18 лет (см. «Способ применения и дозы»).
С осторожностью: пациенты с хронической сердечной недостаточностью I–II функционального класса (в соответствии с классификацией NYHA); возраст 75 лет и старше (см. «Особые указания», «Способ применения и дозы»); заболевания щитовидной железы (см. «Особые указания») — в связи с ограниченным опытом применения.
Наиболее часто регистрируемыми нежелательными реакциями во время клинических исследований являлись нарушения со стороны ЖКТ: тошноту и диарею регистрировали очень часто, а рвоту, запор, боль в животе и диспепсию — часто. В начале терапии препаратом Виктоза® эти нежелательные явления со стороны ЖКТ могут возникать чаще; эти реакции обычно ослабевают в течение нескольких дней или недель на фоне продолжения терапии.
Головную боль и инфекции верхних дыхательных путей также регистрировали часто. Кроме того, гипогликемию регистрировали часто и очень часто при применении препарата Виктоза® в комбинации с производными сульфонилмочевины. Выраженную гипогликемию преимущественно отмечали при комбинированной терапии с производными сульфонилмочевины.
Ниже представлен перечень нежелательных реакций, отмеченных в долгосрочных контролируемых исследованиях III фазы и спонтанных (пострегистрационных) сообщениях. Частота для связанных спонтанных (пострегистрационных) сообщений была рассчитана на основании их частоты в клинических исследованиях IIIа фазы. Нежелательные реакции распределены по группам в соответствии с системами органов MedDRA и частотой. Частота определена следующим образом: очень часто (≥1/10); часто (≥1/100 до <1/10); нечасто (≥1/1000 до <1/100); редко (≥1/10000 до <1/1000); очень редко (<1/10000).
Инфекции и инвазии: часто — инфекции верхних дыхательных путей.
Нарушения иммунной системы: редко — анафилактические реакции.
Нарушения метаболизма и питания: часто — гипогликемия*, анорексия, снижение аппетита; нечасто — дегидратация**.
Со стороны нервной системы: часто — головная боль.
Со стороны сердца: часто — увеличение ЧСС.
Со стороны ЖКТ: очень часто — тошнота, диарея; часто — рвота, диспепсия, боли в верхней части живота, запор, гастрит, метеоризм, вздутие живота, отрыжка; очень редко — панкреатит (включая панкреонекроз).
Со стороны кожи и подкожных тканей: часто — сыпь; нечасто — крапивница, зуд.
Со стороны почек и мочевыводящих путей: нечасто — нарушения функции почек**, острая почечная недостаточность**.
Общие расстройства и реакции в местах введения: часто — реакции в местах введения; нечасто — недомогание.
N=2501 пациент, получающий терапию препаратом Виктоза®
* Явление встречается очень часто при применении в комбинации с инсулином.
** см. «Особые указания».
Описание отдельных побочных реакций
Гипогликемия: большинство эпизодов подтвержденной гипогликемии, зарегистрированных в ходе клинических исследований, были легкими. Во время клинических исследований при применении препарата Виктоза® в виде монотерапии не отмечено случаев возникновения тяжелой гипогликемии. Тяжелая гипогликемия может возникать нечасто и главным образом наблюдаться при применении препарата Виктоза® в комбинации с производными сульфонилмочевины (0,02 случая/пациента в год). При применении препарата Виктоза® в сочетании с другими пероральными гипогликемическими препаратами (не производными сульфонилмочевины) развитие гипогликемии наблюдалось очень редко (0,001 случая/пациента в год).
При терапии препаратом Виктоза® в дозе 1,8 мг в сочетании с инсулином детемир и метформином не было отмечено случаев тяжелых гипогликемий. Частота случаев легкой гипогликемии составила 0,228 случая/пациента в год. В группах пациентов, получавших терапию лираглутидом 1,8 мг и метформином, частота случаев легкой гипогликемии составила 0,034 и 0,115 случая/пациента в год соответственно.
Со стороны ЖКТ: в большинстве случаев тошнота носила легкий или умеренный характер, была преходящей и редко приводила к отмене терапии. Процент пациентов с побочными реакциями в виде тошноты (по неделям) в долгосрочном клиническом исследовании приведен на рис. 3.
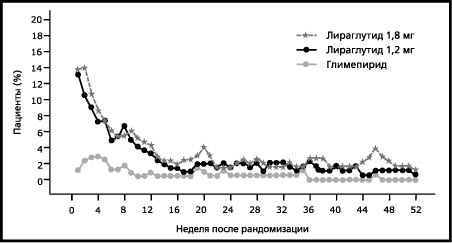
Рисунок 3. Процент пациентов с побочными реакциями в виде тошноты в зависимости от недели — долгосрочное клиническое исследование.
20,7% пациентов, получавших препарат Виктоза® в комбинации с метформином, перенесли минимум один эпизод тошноты, а 12,6% — по крайней мере один эпизод диареи. При приеме препарата Виктоза® в комбинации с производными сульфонилмочевины у 9,1% пациентов отмечен минимум один эпизод тошноты и у 7,9% — по крайней мере по одному случаю развития диареи.
В ходе долгосрочных плацебо-контролируемых клинических исследований (26 нед или более) частота прекращения лечения пациентов из-за появления побочных эффектов составила 7,8% в группе пациентов, получавших препарат Виктоза®, и 3,4% в группе пациентов, получавших препараты сравнения. Наиболее частыми побочными реакциями, которые приводили к прекращению лечения пациентов, получавших препарат Виктоза®, являлись тошнота (2,8% пациентов) и рвота (1,5%).
У пациентов в возрасте старше 70 лет частота развития побочных реакций со стороны ЖКТ при применении препарата Виктоза® может быть выше. При применении препарата Виктоза® у пациентов с легкой и средней степенью почечной недостаточности (Cl креатинина 60–90 и 30–59 мл/мин, соответственно) частота побочных реакций со стороны ЖКТ может быть выше.
Реакции в месте введения: в ходе долгосрочных (26 нед или более) контролируемых исследований приблизительно у 2% субъектов, получавших препарат Виктоза®, отмечались реакции в месте введения препарата. Эти реакции носили, как правило, легкий характер.
Панкреатит: сообщалось о нескольких случаях развития острого панкреатита (<0,2%) в ходе долгосрочных клинических исследований. Имеются сообщения о случаях развития панкреатита в пострегистрационном периоде.
Аллергические реакции: в пострегистрационном периоде сообщалось о возникновении аллергических реакций, таких как крапивница, сыпь и зуд. В пострегистрационном периоде при приеме препарата Виктоза® описано несколько случаев анафилактических реакций, сопровождавшихся такими симптомами, как артериальная гипотония, учащенное сердцебиение, одышка, периферические отеки.
Увеличение ЧСС. Сообщалось о случаях увеличении ЧСС при применении препарата Виктоза®. В долгосрочных клинических исследованиях при применении препарата Виктоза® среднее увеличение ЧСС от исходного уровня составило от 2 до 3 уд./мин.
Долгосрочные клинические последствия не были установлены.
По данным клинических исследований и пострегистрационного применения лираглутида, были зарегистрированы случаи передозировки с увеличением дозы до превышающей рекомендованную дозу в 40 раз (72 мг). Был отмечен один случай передозировки с превышением дозы в 10 раз (18 мг ежедневно) в течение 7 мес.
Симптомы: как правило, пациенты отмечали тяжелую тошноту, рвоту и диарею, но выздоравливали без остаточных явлений. Ни у кого из пациентов не было отмечено гипогликемии тяжелой степени.
Лечение: в случае передозировки препарата Виктоза® рекомендуется проведение соответствующей симптоматической терапии.
Оценка взаимодействия ЛС in vitro. Препарат Виктоза® показал очень низкую способность к фармакокинетическому взаимодействию с ЛС, обусловленному метаболизмом в системе цитохрома Р450 (CYP), а также связыванием с белками плазмы.
Оценка взаимодействия ЛС in vivo. Небольшая задержка в опорожнении желудка при применении препарата Виктоза® может оказывать влияние на всасывание сопутствующих пероральных лекарственных препаратов. Исследования лекарственного взаимодействия не показали какого-либо клинически значимого замедления всасывания этих препаратов. У нескольких пациентов, получавших лечение препаратом Виктоза®, отмечалось минимум по одному эпизоду острой диареи. Диарея может оказывать влияние на всасывание пероральных лекарственных препаратов, которые используются одновременно с препаратом Виктоза®.
Варфарин и другие производные кумарина. Исследования по взаимодействию не проводились. Не может быть исключено клинически значимое взаимодействие с действующими веществами с низкой растворимостью или узким терапевтическим индексом, такими как варфарин. В начале лечения препаратом Виктоза® у пациентов, получающих варфарин или другие производные кумарина, рекомендуется чаще проводить мониторинг MHO.
Парацетамол. Однократное применение парацетамола в дозе 1000 мг на фоне применения препарата Виктоза® не вызывает изменение системной экспозиции. Cmax парацетамола в плазме снизилась на 31%, а среднее Tmax в плазме крови увеличилось на 15 мин. При одновременном применения препарата Виктоза® и парацетамола коррекция дозы последнего не требуется.
Аторвастатин. Однократное применение аторвастатина в дозе 40 мг на фоне применения препарата Виктоза® не вызывает изменение системной экспозиции. Таким образом, на фоне приема препарата Виктоза® коррекция дозы аторвастатина не требуется. Cmax аторвастатина в плазме снизилась на 38%, а среднее значение Tmax в плазме на фоне применения препарата Виктоза® увеличилось с 1 до 3 ч.
Гризеофульвин. Однократное применение гризеофульвина в дозе 500 мг на фоне применения препарата Виктоза® не вызывает изменение системной экспозиции. Cmax гризеофульвина возросла на 37%, в то время как среднее значение Tmax в плазме не изменилось. Коррекция дозы гризеофульвина и других ЛС, имеющих низкую растворимость и высокую проницаемость, не требуется.
Дигоксин. При одновременном однократном введении дигоксина в дозе 1 мг и препарата Виктоза® отмечалось уменьшение AUC дигоксина на 16%; Cmax дигоксина снизилась на 31%. Среднее значение Tmax дигоксина в плазме увеличилось с 1 до 1,5 ч. Исходя из полученных результатов, коррекция дозы дигоксина на фоне применения препарата Виктоза® не требуется.
Лизиноприл. Однократное применение лизиноприла в дозе 20 мг на фоне применения препарата Виктоза® привело к уменьшению AUC лизиноприла на 15%; Cmax лизиноприла снизилась на 27%. Среднее значение Tmax лизиноприла в плазме на фоне применения препарата Виктоза® увеличилось с 6 до 8 ч. Исходя из полученных результатов, коррекция дозы лизиноприла на фоне приема лираглутида не требуется.
Пероральные контрацептивы. Cmax этинилэстрадиола и левоноргестрела после их однократного применения на фоне терапии препаратом Виктоза® снизилась на 12 и 13% соответственно. Применение обоих препаратов вместе с препаратом Виктоза® сопровождалось увеличением Tmax этих ЛС на 1,5 ч. Клинически значимый эффект на системную экспозицию этинилэстрадиола и левоноргестрела в организме лираглутид не оказывает. Таким образом, ожидаемый контрацептивный эффект обоих ЛС на фоне терапии препаратом Виктоза® не изменяется.
Инсулин. Не было выявлено фармакокинетическое или фармакодинамическое взаимодействие препарата Виктоза® с инсулином детемир при однократном применении инсулина детемир в дозе 0,5 ЕД/кг с препаратом Виктоза® в дозе 1,8 мг у пациентов с сахарным диабетом типа 2.
Несовместимость. Вещества, добавленные к препарату Виктоза®, могут вызвать деградацию лираглутида. Препарат Виктоза® нельзя смешивать с другими ЛС, в т.ч. с инфузионными растворами.
Препарат Виктоза® не следует использовать у пациентов с сахарным диабетом типа 1 или для лечения диабетического кетоацидоза.
Препарат Виктоза® не заменяет инсулин.
Опыт применения препарата Виктоза® у пациентов с сердечной недостаточностью I–II функциональных классов в соответствии с функциональной классификацией ХСН NYHA ограничен, поэтому у этих пациентов препарат следует применять с осторожностью. Отсутствует опыт применения препарата Виктоза® у пациентов с ХСН III–IV функциональных классов в соответствии с классификацией ХСН NYHA. Применение препарата Виктоза® у таких пациентов противопоказано.
Опыт применения препарата Виктоза® у пациентов с воспалительными заболеваниями кишечника и диабетическим парезом желудка ограничен, поэтому применение препарата Виктоза® у данных групп больных противопоказано, т.к. ассоциируется с развитием преходящих побочных реакций со стороны ЖКТ, таких как тошнота, рвота и диарея.
Острый панкреатит
Применение агонистов ГПП-1 ассоциировалось с риском развития острого панкреатита. Сообщалось о развитии острого панкреатита в ходе клинических исследований и пострегистрационном периоде. Пациенты должны быть информированы о характерных симптомах острого панкреатита. При подозрении на панкреатит терапия препаратом Виктоза® должна быть немедленно прекращена; в случае подтверждения острого панкреатита терапию препаратом Виктоза® возобновлять не следует. Следует соблюдать осторожность при применении препарата у пациентов с панкреатитом в анамнезе.
Заболевания щитовидной железы
В ходе клинических исследований препарата Виктоза® у отдельных пациентов (в частности у пациентов, уже имеющих заболевания щитовидной железы) сообщалось о побочных явлениях со стороны щитовидной железы, включая повышение концентрации кальцитонина в сыворотке крови, зоб и новообразования щитовидной железы, в связи с этим препарат Виктоза® у таких пациентов следует применять с осторожностью (см. «С осторожностью»).
В постмаркетинговом периоде у пациентов, получавших лираглутид, были отмечены случаи медуллярного рака щитовидной железы. Имеющихся данных недостаточно для установления или исключения причинно-следственной связи возникновения медуллярного рака щитовидной железы с применением лираглутида у человека. Необходимо проинформировать пациента о риске медуллярного рака щитовидной железы и симптомах опухоли щитовидной железы (уплотнения в области шеи, дисфагия, одышка, непроходящая охриплость голоса).
Гипогликемия
Пациенты, получающие препарат Виктоза® в комбинации с производными сульфонилмочевины или базальным инсулином, имеют повышенный риск развития гипогликемии (см. «Побочное действие»). Риск развития гипогликемии можно снизить, уменьшив дозу производных сульфонилмочевины или базального инсулина.
Дегидратация
В ходе проведения клинических исследований сообщалось о появлении признаков и симптомов дегидратации и почечной недостаточности у пациентов, принимавших препарат Виктоза®. Пациенты, получающие препарат Виктоза®, должны быть предупреждены о возможном риске обезвоживания в связи с побочными эффектами со стороны ЖКТ и о необходимости соблюдения ими мер предосторожности, чтобы избежать развития гиповолемии.
Фертильность
За исключением небольшого уменьшения числа живых имплантатов, в исследованиях на животных не было получено свидетельств неблагоприятного влияния на фертильность.
Влияние на способность управлять транспортными средствами и работу с механизмами. Исследований влияния препарата Виктоза® на способность управлять транспортными средствами и работать с механизмами не проводилось. Маловероятно, что препарат Виктоза® может влиять на способность управлять транспортными средствами или работать с механизмами. Пациенты должны быть предупреждены о том, что им следует соблюдать меры предосторожности во избежание развития у них гипогликемии во время управления транспортными средствами и при работе с механизмами, особенно при применении препарата Виктоза® в комбинации с производными сульфонилмочевины или базальным инсулином.
Руководство по использованию
Шприц-ручка Виктоза® предназначена только для индивидуального использования. Препарат Виктоза® нельзя использовать, если он выглядит иначе, чем прозрачная и бесцветная или почти бесцветная жидкость.
Препарат Виктоза® нельзя использовать, если он подвергся замораживанию.
Препарат Виктоза® можно вводить при помощи игл длиной до 8 мм и толщиной до 32G.
Шприц-ручка предназначена для использования в комбинации с одноразовыми инъекционными иглами НовоФайн® или НовоТвист®.
Инъекционные иглы не включены в упаковку. Пациент должен быть проинформирован о том, что использованную иглу следует выбрасывать после каждой инъекции, а также о том, что нельзя хранить шприц-ручку с присоединенной иглой. Такая мера позволит предотвратить загрязнение, инфицирование и утечку препарата из шприц-ручки и гарантирует точность дозирования.
Раствор для подкожного введения 6 мг/мл. По 3 мл в картриджи из стекла 1 гидролитического класса, укупоренные диском из бромбутиловой резины/полиизопрена с одной стороны и поршнем из бромбутиловой резины с другой.
Картридж запаян в пластиковую одноразовую шприц-ручку для многократных инъекций. По 1, 2 или 3 пластиковых одноразовых шприц-ручки для многократных инъекций в картонной пачке.
В каждой шприц-ручке (3 мл) содержится 30 доз по 0,6 мг, 15 доз по 1,2 мг или 10 доз по 1,8 мг лираглутида.
По рецепту.
Производитель и владелец регистрационного удостоверения: Ново Нордиск А/С.
Ново Алле, DK-2880, Багсваерд, Дания.
www.novonordisk.com
Претензии потребителей направлять по адресу: ООО «Ново Нордиск». 121614, Москва, ул. Крылатская, 15, оф. 41.
Тел.: (495) 956-11-32; факс: (495) 956-50-13.
www.novonordisk.ru